PAlA Biotech
PAlA Biotech成立于2014年,位于德国科隆,是基于其专有微孔板技术的抗体和蛋白质微珠分析的创新者,为其检测技术开发了不断增长的高通量检测产品组合,使用小体积的特殊微孔板。已推出多条产品线,包括用于生物制剂发现和开发的基于板的检测试剂盒解决方案,用于抗体发现的成药性检测,高通量错配、聚集、游离寡糖和滴度分析。此外,PAIA Biotech还提供聚糖筛选分析服务,可以满足细胞培养实验室的样本数量和周转要求。

抗体已经成为当代生物医药重点组成部分。而在抗体药物研发生产过程中,一种打破传统,更加高通量,更加快速的抗体滴度检测,抗体错配分析,抗体聚集程度检测,抗体糖基化分析,抗体表面疏水性检测,抗体表面电荷检测,抗体多特异性检测,抗体胞饮作用检测方法的广泛应用,将极大的提高抗体行业的发展。PAlA Biotech基于其专有微孔板技术开发的系列检测试剂盒,正是这样一种打破传统的好产品。
PAIA biotech微孔板技术原理
我们以高通量抗体滴度筛选试剂盒为例,来进行PAlA Biotech的系列检测试剂盒原理说明。
PAlA Biotech在中间突起的孔里预先加入微球,微球上带有Fc结构。由于微孔板中间突起,因此在重力作用下微球位于孔板底部。向微孔中加入带有荧光集团的proteinA,然后加入样本,并进行混匀。样本中的抗体分子会和带有荧光集团的proteinA结合,并存在溶液中。而未被样本中抗体结合的proteinA分子将被带有Fc结构的微球结合,并沉淀于微孔底部。
透过微孔板底部进行荧光分析,基于荧光值得大小即可判定样本中抗体滴度的大小。
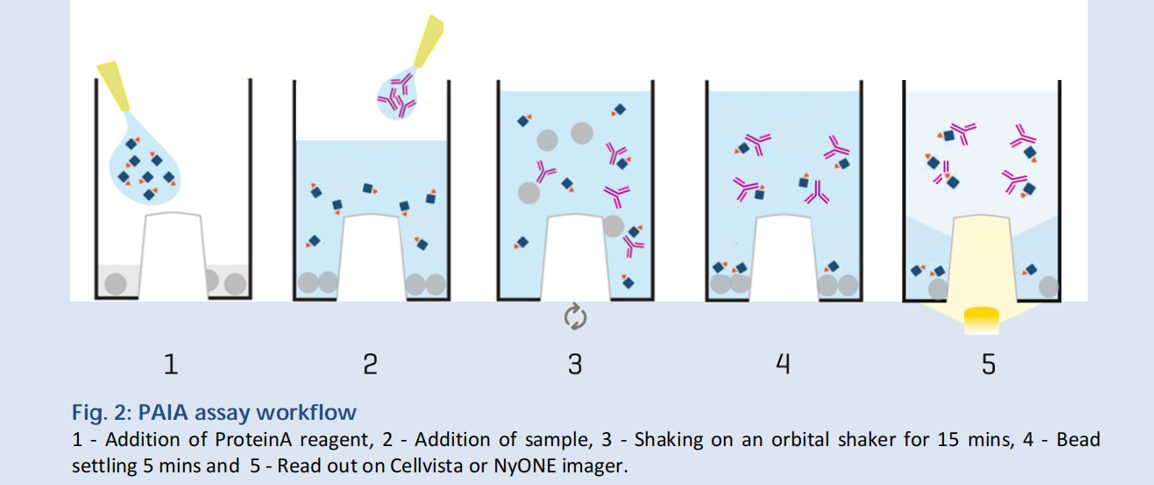
基于此原理,PAlA Biotech还开发了抗体错配分析、聚集程度检测、糖基化分析、表面疏水性检测、表面电荷检测、多特异性检测及胞饮作用检测系列试剂盒。这些基于微孔法的检测试剂盒,相对于传统的检测方法,通量更大、检测速度更快,并且可以兼容自动化系统,节省更多人力成本。
PAIA biotech产品应用介绍
应用场景一、PAIA biotech产品用于抗体滴度检测
检测原理:如上文介绍
传统抗体检测方法包括:
1. 酶联免疫吸附测定(ELISA)
· 原理:利用抗原-抗体的特异性结合,结合酶标二抗和显色反应,通过比色法检测抗体浓度。
· 优点:灵敏度高,适用于低浓度的抗体检测。
· 缺点:操作步骤繁琐,耗时长,洗涤和孵育时间较长,且结果易受实验人员操作的影响,难以实现高通量。
2. 高效液相色谱 (HPLC) - 蛋白A亲和色谱
· 原理:使用Protein A亲和色谱柱,通过抗体的Fc区与Protein A的结合特性分离和定量抗体。
· 优点:灵敏度高,特异性强,尤其适用于纯化过程中的抗体浓度检测。
· 缺点:设备昂贵,操作复杂,检测周期长,无法高通量操作。
3. 表面等离子共振(SPR)
· 原理:利用表面等离子共振技术,实时监测抗原-抗体结合的动力学变化,从而定量检测抗体滴度。
· 优点:可实时监测,数据稳定,能够测定结合动力学参数。
· 缺点:设备昂贵,操作复杂,样品用量大,难以高通量处理。
4. 电泳/Western Blot
· 原理:通过SDS-PAGE分离蛋白质,然后用抗体与蛋白结合,并通过化学发光或显色系统检测抗体的存在。
· 优点:可分析抗体的分子量和结构信息,操作方法成熟。
· 缺点:无法精确定量,操作耗时,灵敏度不高,重复性差,难以高通量检测。
5. 紫外-可见分光光度计(UV-Vis)
· 原理:通过在280 nm处检测抗体溶液的吸光度(A280)来定量蛋白质浓度。
· 优点:快速、简单、无损伤,适用于大规模的在线监测。
· 缺点:特异性差,无法区分抗体与其他蛋白质,难以高通量操作。
6. 毛细管电泳(CE-SDS)
· 原理:通过电泳分离蛋白质,结合SDS,定量检测抗体浓度。
· 优点:高分辨率,可同时检测抗体的纯度和分子量。
· 缺点:仪器昂贵,操作复杂,无法高通量检测。
PAIA biotech与传统方法的对比总结
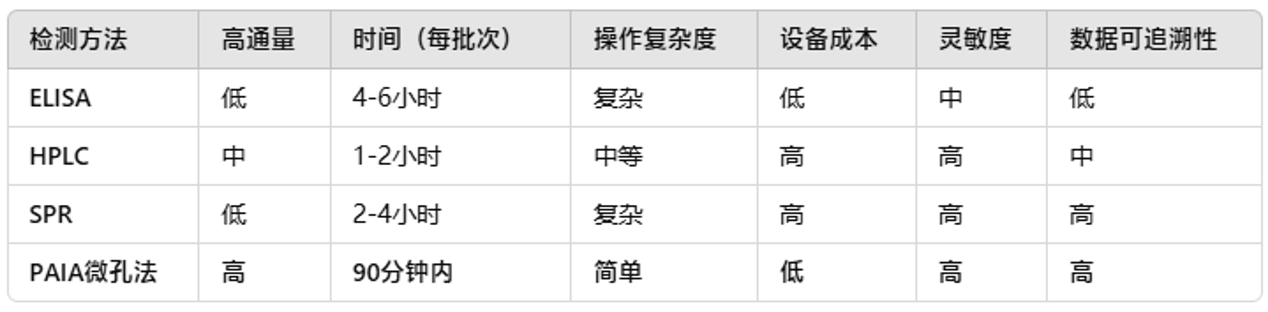
总的来说,其与传统方法相比,更快、更简便、效率更高,尤其适用于规模生产和GMP环境中的批量检测。
应用场景二、PAIA biotech产品用于抗体糖基化分析
检测原理:同样基于中间突起的微孔板,将样品(如抗体或糖蛋白)加入PAIA的微孔板中,孔内预包被了特异性糖结合分子(如凝集素),这些分子可特异性识别并结合到目标糖基(如甘露糖、半乳糖、唾液酸等)上。加入标记了荧光的二抗或其他荧光探针,特异性识别与目标糖基结合的分子。利用荧光读板仪读取荧光信号,荧光强度与样品中糖基的丰度呈正相关。
传统的糖基化检测方法包括:
1. 高效液相色谱-糖肽分析 (HPLC-Glycan Profiling)
· 原理:先对抗体进行酶解,释放出N-糖或O-糖后,使用荧光标记法标记糖基,再通过HPLC分离糖基,并检测其荧光信号。
· 优点:可以精确分析和定量目标糖基的组成和丰度,分离度高。
· 缺点:流程繁琐,操作复杂,通常需要1-2天才能完成,成本高,无法高通量处理。
2. 质谱检测 (LC-MS/MS, MALDI-TOF-MS)
· 原理:将抗体的糖基分离后,采用**液相色谱-质谱联用(LC-MS/MS)或基质辅助激光解吸电离飞行时间质谱(MALDI-TOF-MS)**检测糖基的质量和序列。
· 优点:可以提供高分辨率的糖基结构信息,能够区分同分异构体,精确度高。
· 缺点:设备昂贵,技术要求高,数据解析复杂,无法大规模高通量筛选,检测周期长(通常2-3天)。
3. 毛细管电泳 (CE-LIF) - 荧光标记糖基法
· 原理:将糖基通过荧光标记后,利用毛细管电泳在电场中分离糖分子,使用激光诱导荧光(LIF)检测信号。
· 优点:灵敏度高,分析速度快,分离度高。
· 缺点:设备成本高,方法复杂,通常需要1天或更长时间,无法高通量操作。
4. 凝集素芯片(Lectin Array)
· 原理:利用凝集素(如ConA、WGA等)对糖基的特异性识别和结合,将这些凝集素固定在芯片上,通过荧光检测样品中的糖基化特征。
· 优点:能够多重检测多种糖基化修饰,并可一次性分析多个样品中的多种糖基类型。
· 缺点:设备和试剂成本高,数据解释复杂,灵敏度低于质谱,无法量化特定的糖基数量。
5. ELISA方法(Enzyme-Linked Lectin Assay, ELLA)
· 原理:在ELISA板中包被目标糖基,加入抗体,随后通过特异性抗糖基抗体和酶联反应显色,最终通过比色法检测样品中糖基的含量。
· 优点:方法成熟、成本低、特异性高,适用于定量检测。
· 缺点:灵敏度较低,无法检测低丰度糖基修饰,操作流程复杂,检测时间长(4-6小时),且难以高通量。
PAIA biotech与传统方法的对比总结
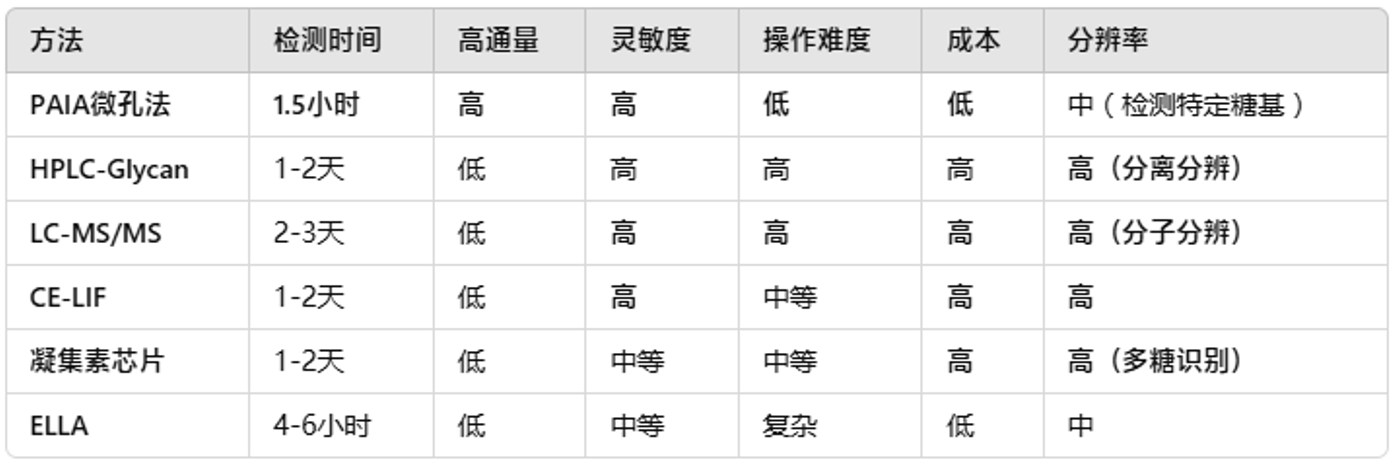
总的来说,PAIA的微孔平台通过高通量、快速和免洗的检测技术,在糖基化检测中表现优异。与HPLC、质谱和毛细管电泳等传统方法相比,PAIA的速度更快、成本更低、操作更简单,尤其适用于生产环境和大规模筛选。
应用场景三、PAIA biotech产品用于抗体错配检测
PAIA biotech产品用于抗体错配检测的原理
在生物制药和抗体药物开发过程中,抗体错配(mismatch)是一个常见的问题,尤其在抗体筛选、生产和质控阶段。
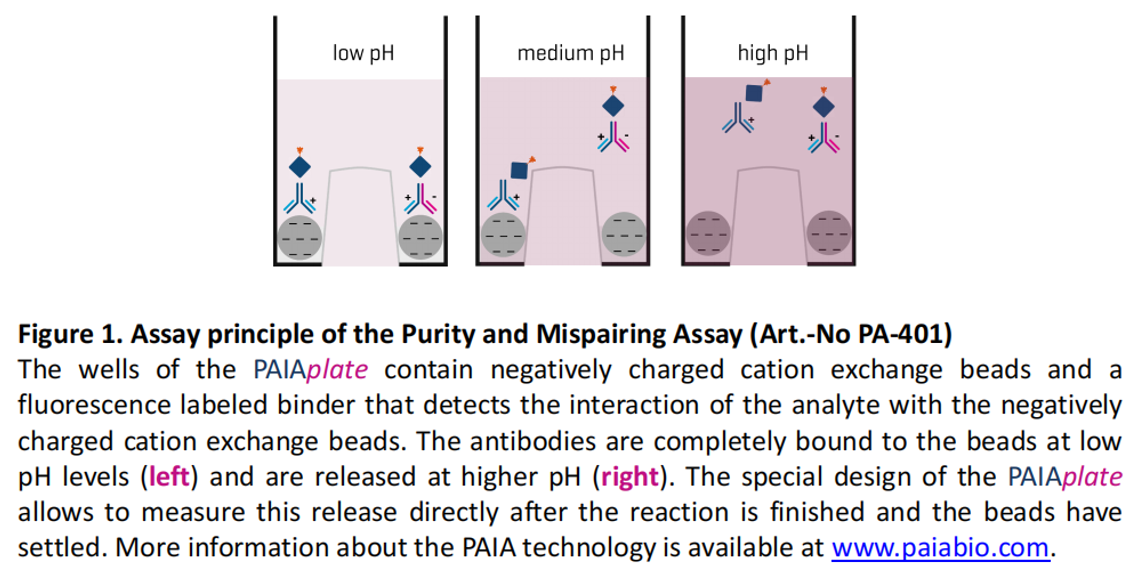
PAIA biotech的试剂盒,同样借助中间突起的微孔板,基于在不同的PH的情况下,错配和正确配对的抗体,他们对离子交换磁珠的结合能力是不同的为原理,因此会显示出不同的荧光读数量,依次判定样本中抗体的错配情况。
传统的抗体错配检测方法
传统方法主要包括ELISA(酶联免疫吸附法)、HPLC(高效液相色谱法)和SPR(表面等离子共振法)等技术。每种方法的检测原理和操作流程各不相同,具体如下:
1. ELISA(酶联免疫吸附法)
· 原理:ELISA利用抗原-抗体的特异性结合反应,在微孔板上对抗体的结合能力进行检测。通常,靶抗原会被固定在微孔板的底部,当加入抗体样品后,特定的抗体会与抗原结合。为了检测这种结合反应,加入与抗体结合的标记二抗(通常是HRP标记的二抗)。通过加入底物(如TMB溶液)并在特定条件下显色,显色强度与结合的抗体数量成正比。
· 操作流程:包被抗原 → 封闭 → 加入样品 → 加入二抗 → 显色反应 → 终止反应 → 读板检测。
· 优点:灵敏度高、操作设备简单,适用于大规模样品筛选和质控检测。
· 缺点:操作步骤繁琐,检测时间较长(3-5小时),需要多次洗涤,容易出现假阳性或假阴性。
2. HPLC(高效液相色谱法)
· 原理:HPLC是一种基于分子尺寸、极性或电荷差异的分离检测技术。样品在高压泵的推动下通过固定相填充的色谱柱,不同成分因物理化学特性的不同,在色谱柱中被分离。HPLC可以分离和检测不同的抗体亚型、抗体聚集体和杂质等,从而区分抗体错配现象。
· 操作流程:样品前处理 → 进样 → 通过色谱柱分离 → 通过检测器检测(如紫外/荧光检测器) → 数据记录与分析。
· 优点:灵敏度高,适用于检测抗体分子量、纯度、聚集体及其结构差异。
· 缺点:操作复杂,样品前处理繁琐,检测时间较长(2-4小时),设备成本高,难以实现高通量检测。
3. SPR(表面等离子共振法)
· 原理:SPR是一种实时监测分子间相互作用动力学的技术,基于光在金属界面反射时的表面等离子体共振现象。检测时,将一种分子(如抗原)固定在金属表面,另一种分子(如抗体)通过流动样品与之结合。分子结合引起表面折射率的变化,SPR传感器记录到的共振角变化与分子结合的数量成正比,从而监测到结合的抗体。
· 操作流程:抗原固定 → 流动样品(抗体)注入 → 动态实时监测分子结合情况 → 数据记录与分析。
· 优点:实时检测、动态监测,灵敏度高,能提供结合动力学数据(如Ka、Kd)。
· 缺点:成本高,设备昂贵,操作复杂,通常单次只能检测一个样品,难以高通量操作。
PAIA biotech检测试剂盒与传统方法的对比总结
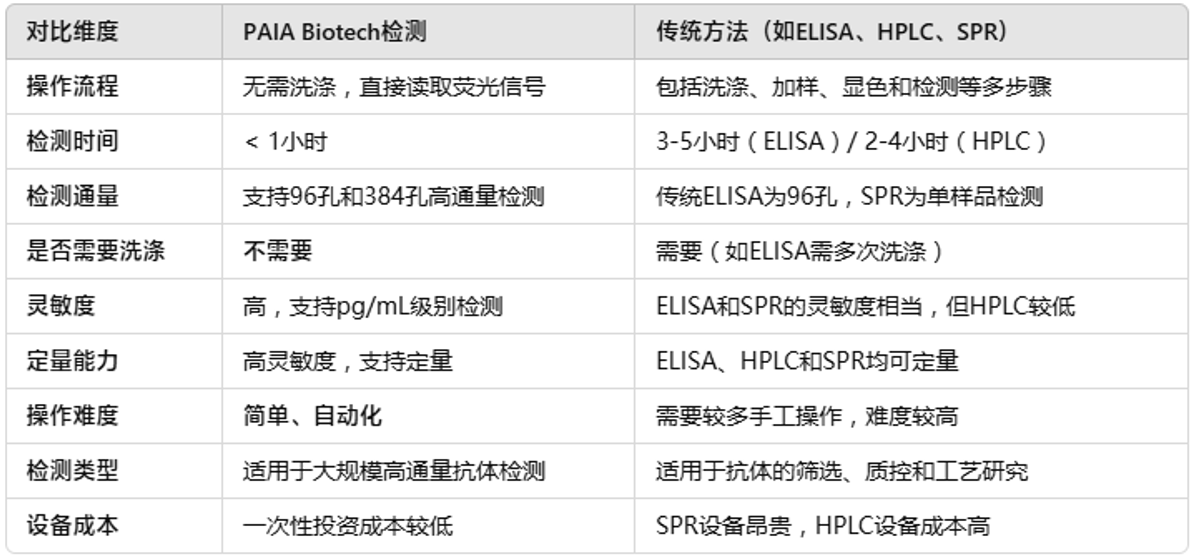
总的来说,PAIA Biotech的检测技术在高通量、快速、简单操作等方面具有显著优势,特别适合用于大规模的抗体错配检测。与传统的ELISA和HPLC方法相比,PAIA检测缩短了检测时间,降低了操作复杂性,并且对高通量的抗体筛选和生产环境更加友好。
应用场景四、PAIA biotech产品用于抗体聚集分析
抗体聚集体的产生可能会影响药物的安全性、稳定性和有效性。抗体药物开发,质量控制(QC),工艺优化流程都需要进行抗体聚集检测分析。
PAIA biotech产品用于抗体聚集检测原理
PAIA Biotech的抗体聚集检测采用了荧光微孔板检测技术,其核心原理是利用特异性配体(如捕获抗体或结合分子)在微孔板中捕获抗体聚集体,并通过荧光标记的二抗对其进行可视化检测。将抗体样品加入特定配体包被的微孔板中,聚集体会优先与捕获分子结合,入荧光标记的二抗,二抗与捕获的抗体聚集体结合,产生可检测的荧光信号,荧光检测仪对每个孔的荧光强度进行读取,荧光强度的高低与抗体聚集体的数量成正比。
传统的抗体聚集分析方法及其局限性
传统的抗体聚集检测方法主要包括SEC-HPLC(凝胶过滤色谱法)、DLS(动态光散射)和AUC(分析超速离心)等。这些方法的原理和检测特点如下:
1. SEC-HPLC(凝胶过滤色谱法)
· 原理:SEC-HPLC利用抗体分子的分子大小差异进行分离,较大的分子(聚集体)会更早从色谱柱中流出,而较小的单体则滞后流出,从而实现分离和检测。
· 局限性:
1)检测速度慢,通常每个样品检测需要30分钟到1小时。
2)样品前处理复杂,需要脱气、过滤等操作,增加了人力成本。
3)高压操作可能破坏天然的抗体聚集体,造成检测偏差。
2. DLS(动态光散射)
· 原理:DLS是通过分析样品中颗粒的布朗运动速率,计算出颗粒的粒径分布。抗体聚集体的体积比单体更大,光的散射强度也更高,因此可通过散射信号区分抗体单体和聚集体。
· 局限性:
1)对高浓度样品不敏感,高浓度的蛋白溶液容易引发多重散射效应,导致数据不准确。
2)只适用于检测较大的颗粒,无法区分微小的抗体二聚体或寡聚体。
3)只能测量体积信息,无法获得抗体的定量信息。
3. AUC(分析超速离心)
· 原理:AUC通过在高离心力下将样品中不同质量的分子分离,抗体单体、二聚体和更高聚集体会分离成不同的带。
· 局限性:
1)检测设备昂贵,操作复杂,通常需要经过专门培训的人员操作。
2)检测过程耗时长达6-8小时,不适合高通量分析。
3)只能在低样品通量下操作,无法应对大规模样品检测需求。
PAIA Biotech的抗体聚集检测优势
与传统的抗体聚集分析方法相比,PAIA Biotech的检测方案在速度、成本和通量方面具有较大优势。
· 检测速度快:与SEC-HPLC和AUC相比,PAIA检测通常在1小时内完成,可大幅缩短检测时间。
· 高通量检测:PAIA检测平台支持96孔和384孔板,实现批量检测,而SEC-HPLC和AUC只能单样品逐一检测。
· 无需洗涤,自动化程度高:PAIA检测过程不需要洗涤步骤,自动化平台可快速操作,节省人力和时间成本。
· 灵敏度高:可检测到pg/mL级别的抗体浓度,尤其适用于早期药物筛选和大规模质控。
· 简单的设备要求:与SPR和AUC所需的昂贵设备不同,PAIA只需标准的荧光微孔板检测仪,维护成本低、便于操作。
PAIA biotech检测试剂盒与传统方法的对比总结
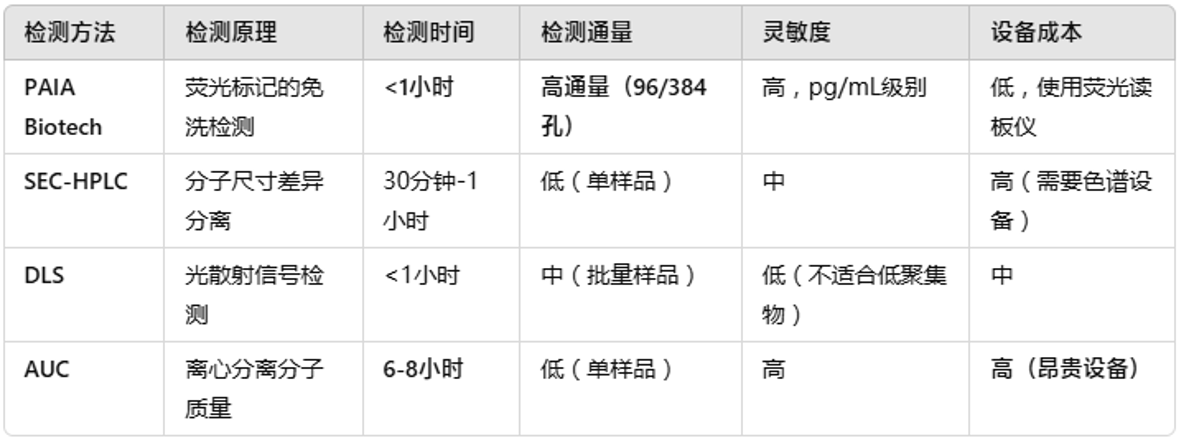
PAIA Biotech的抗体聚集检测优势
与传统的抗体聚集分析方法相比,PAIA Biotech的检测方案在速度、成本和通量方面具有较大优势。
· 检测速度快:与SEC-HPLC和AUC相比,PAIA检测通常在1小时内完成,可大幅缩短检测时间。
· 高通量检测:PAIA检测平台支持96孔和384孔板,实现批量检测,而SEC-HPLC和AUC只能单样品逐一检测。
· 无需洗涤,自动化程度高:PAIA检测过程不需要洗涤步骤,自动化平台可快速操作,节省人力和时间成本。
· 灵敏度高:可检测到pg/mL级别的抗体浓度,尤其适用于早期药物筛选和大规模质控。
· 简单的设备要求:与SPR和AUC所需的昂贵设备不同,PAIA只需标准的荧光微孔板检测仪,维护成本低、便于操作。
应用场景五、PAIA biotech产品用于抗体表面疏水性检测,抗体表面电荷检测,抗体多特异性检测,抗体胞饮作用检测
PAIA biotech同样基于荧光微孔板检测技术,开发了抗体表面疏水性检测,抗体表面电荷检测,抗体多特异性检测,抗体胞饮作用检测系列试剂盒。我们以抗体表面疏水性检测,抗体表面电荷检测为例,进行相关产品介绍。
抗体表面疏水性检测
首先抗体表面疏水性检测方面,抗体表面疏水性的评估对于预测抗体的聚集风险、稳定性和可开发性至关重要。传统的检测方式有反相高效液相色谱(RP-HPLC),表面等离子体共振(SPR),疏水相互作用色谱(HIC, Hydrophobic Interaction Chromatography)等。与传统方式相比,PAIA biotech产品具有如下优点:
· 高通量:
1)支持96孔/384孔板操作,一次可同时检测数十至上百个抗体样品。
2)与传统的HPLC、SPR、HIC方法相比,检测速度更快,适合大规模的抗体库筛选。
· 快速检测,1小时内完成:
传统HPLC和HIC方法需要几个小时,而PAIA方法在1小时内即可完成检测,节省时间成本。
· 无需复杂仪器,操作简单:
不需要使用HPLC、SPR等昂贵的精密仪器,只需普通的荧光检测仪,大大降低了设备和维护成本。
· 无洗涤操作,节省人力:
传统的疏水性检测(如HIC)需要多步洗涤和洗脱,而PAIA的检测方案不需要洗涤操作,大大减少了操作步骤和人工干预。
· 检测灵敏度高,结果稳定:
与传统的ANS荧光染料法相比,PAIA的荧光标记技术更加敏感,能够检测到更小的疏水性差异,结果可重复性更高。
· 样品用量少,节约成本:
PAIA的检测中,每孔的样品需求量非常少(仅需10-50 μL),与SPR和HIC等高样品需求的传统技术形成对比,降低了检测成本。
· 适合抗体开发中的早期筛选:
在候选抗体的开发过程中,PAIA的高通量检测能力帮助筛选疏水性较低的抗体变体,减少后续的聚集风险。
抗体表面电荷检测
抗体表面电荷检测方面,抗体表面电荷同样是影响抗体稳定性、可溶性和药代动力学特性的关键因素。电荷的变化可能导致聚集、吸附和效价下降。
传统的抗体表面电荷检测方法包括等电聚焦电泳(IEF, Isoelectric Focusing),毛细管区带电泳(CZE, Capillary Zone Electrophoresis),离子交换色谱(IEC, Ion Exchange Chromatography)等
与传统方式相比,PAIA biotech产品具有如下优点: